Νευρολογικές παθήσεις | Dr. Θεοδώρα Γιολτζόγλου Ειδικός Νευρολόγος Θεσσαλονίκη
►
▼
Η νόσος Πάρκινσον
Η νόσος Πάρκινσον είναι μια νευροεκφυλιστική διαταραχή της οποίας τα βασικά κλινικά χαρακτηριστικά είναι ο τρόμος ηρεμίας, η δυσκαμψία, η βραδυκινησία, η διαταραχή της βάδισης και της ισορροπίας. Χαρακτηρίζεται παθολογοανατομικά από εκλεκτική εκφύλιση των ντοπαμινεργικών νευρώνων του συμπαγούς τμήματος της μέλαινας ουσίας σε συνδυασμό με την εμφάνιση ενδοκυτταροπλασματικών εγκλείστων που αποτελούνται από συνάθροισμα πρωτεϊνών, που είναι γνωστά ως σωμάτια Lewy. Νευροεκφύλιση παρατηρείται επίσης και σε άλλες περιοχές του εγκεφάλου, όπως τον υπομέλανα τόπο, τους πυρήνες της ραφής, τον βασικό πυρήνα του Meynert, τον υποθάλαμο, τον φλοιό, πυρήνες κρανιακών νεύρων και στοιχεία του αυτονόμου.
Στις βιομηχανοποιημένες χώρες 0,3%, του γενικού πληθυσμού και 1% των ατόμων άνω των 60 ετών πάσχουν από νόσο Πάρκινσον [18]. Είναι λιγότερο συχνή σε μαύρους και ασιάτες από ότι στους λευκούς και οι μάλλον, συχνότερη στους άντρες [25], [24], [22], ίσως λόγω της προστατευτικής δράσης των οιστρογόνων στις στις γυναίκες .
Η έναρξη της νόσου είναι σπάνια σε ηλικίες κάτω των 50 και υπάρχει σχεδόν κάθετη αύξηση μετά τα 60.
Διάγνωση της νόσου του Πάρκινσον
Η διάγνωση της νόσου του Πάρκινσον είναι κατά βάση κλινική, ενώ εργαστηριακές εξετάσεις μπορεί να απαιτούνται για να αποκλείσουν νοσήματα που μιμούνται την νόσο.
Διαβάστε περισσότερα
Στις βιομηχανοποιημένες χώρες 0,3%, του γενικού πληθυσμού και 1% των ατόμων άνω των 60 ετών πάσχουν από νόσο Πάρκινσον [18]. Είναι λιγότερο συχνή σε μαύρους και ασιάτες από ότι στους λευκούς και οι μάλλον, συχνότερη στους άντρες [25], [24], [22], ίσως λόγω της προστατευτικής δράσης των οιστρογόνων στις στις γυναίκες .
Η έναρξη της νόσου είναι σπάνια σε ηλικίες κάτω των 50 και υπάρχει σχεδόν κάθετη αύξηση μετά τα 60.
Διάγνωση της νόσου του Πάρκινσον
Η διάγνωση της νόσου του Πάρκινσον είναι κατά βάση κλινική, ενώ εργαστηριακές εξετάσεις μπορεί να απαιτούνται για να αποκλείσουν νοσήματα που μιμούνται την νόσο.
Διαβάστε περισσότερα
Η νόσος Πάρκινσον είναι μια νευροεκφυλιστική διαταραχή της οποίας τα βασικά κλινικά χαρακτηριστικά είναι ο τρόμος ηρεμίας, η δυσκαμψία, η βραδυκινησία, η διαταραχή της βάδισης και της ισορροπίας. Χαρακτηρίζεται παθολογοανατομικά από εκλεκτική εκφύλιση των ντοπαμινεργικών νευρώνων του συμπαγούς τμήματος της μέλαινας ουσίας σε συνδυασμό με την εμφάνιση ενδοκυτταροπλασματικών εγκλείστων που αποτελούνται από συνάθροισμα πρωτεϊνών, που είναι γνωστά ως σωμάτια Lewy. Νευροεκφύλιση παρατηρείται επίσης και σε άλλες περιοχές του εγκεφάλου, όπως τον υπομέλανα τόπο, τους πυρήνες της ραφής, τον βασικό πυρήνα του Meynert, τον υποθάλαμο, τον φλοιό, πυρήνες κρανιακών νεύρων και στοιχεία του αυτονόμου.
Στις βιομηχανοποιημένες χώρες 0,3%, του γενικού πληθυσμού και 1% των ατόμων άνω των 60 ετών πάσχουν από νόσο Πάρκινσον [18]. Είναι λιγότερο συχνή σε μαύρους και ασιάτες από ότι στους λευκούς και οι μάλλον, συχνότερη στους άντρες [25], [24], [22], ίσως λόγω της προστατευτικής δράσης των οιστρογόνων στις στις γυναίκες .
Η έναρξη της νόσου είναι σπάνια σε ηλικίες κάτω των 50 και υπάρχει σχεδόν κάθετη αύξηση μετά τα 60.
Διάγνωση της νόσου του Πάρκινσον
Η διάγνωση της νόσου του Πάρκινσον είναι κατά βάση κλινική, ενώ εργαστηριακές εξετάσεις μπορεί να απαιτούνται για να αποκλείσουν νοσήματα που μιμούνται την νόσο.
Τα θεμελιώδη χαρακτηριστικά της νόσου είναι η βραδυκινησία, ο τρόμος ηρεμίας και η δυσκαμψία, ενώ η αστάθεια είναι μη ειδική και σπάνια εμφανίζεται στην έναρξη της νόσου.
Η βραδυκινησία είναι, ίσως το πιο ενοχλητικό σύμπτωμα της πρώιμης νόσου. Εκδηλώνεται αρχικά με δυσκολία στις λεπτές κινήσεις, όπως το κούμπωμα των κουμπιών ή το γράψιμο και με την μείωση των αιωρήσεων των άκρων στην βάδιση.
Ο τρόμος ηρεμίας(τρέμουλο) με συχνότητα τυπικά 4-6 Hz (τρόμος καταμέτρησης καταποτίων ή κερμάτων, “pillrolling”) έχει συνήθως ασύμμετρη έναρξη και χειροτερεύει με το άγχος, την ετερόπλευρη κινητική δραστηριότητα και κατά την βάδιση.
Η δυσκαμψία είναι η συνεχής και ομοιόμορφη αύξηση του μυϊκού τόνου.
Η αστάθεια αναφέρεται στην σταδιακή ανάπτυξη διαταραχής ισορροπίας, που οδηγεί σε αυξημένο κίνδυνο πτώσεων.
Ο ασθενής συνήθως αντιλαμβάνεται την έναρξη της νόσου, ως δυσκολία στις λεπτές κινήσεις, όπως στο κούμπωμα ή το ξύρισμα, ένα ήπιο τρέμουλο σε ένα χέρι και υποκειμενική (αρχικά) αστάθεια στην βάδιση.
Πολύ νωρίτερα, εμφανίζονται συμπτώματα που είναιπροκλινικά χαρακτηριστικά της νόσου και παλαιότερα θεωρούνταν «παράγοντες κινδύνου» για την ανάπτυξη της νόσου.
Τα πλέον πρώιμα από αυτά είναι η δυσκοιλιότητα και η διαταραχή της όσφρησης. Ακολουθούν, οι διαταραχές του ύπνου, διάφορα σύνδρομα πόνου, όπως κεφαλαλγίες, άγχος, διαταραχή πανικού, μειωμένη ικανότητα διαχείρισης του άγχους, συναισθηματικές διαταραχές, βραδύτητα σκέψης, κατάθλιψη, κόπωση, παροδικά κινητικά συμπτώματα και γνωστικά ελλείμματα.
Παρότι δεν υπάρχουν μεγάλες προοπτικές μελέτες που να το αποδεικνύουν, φαίνεται ότι οι ασθενείς με πρώιμη ή υποκλινική νόσο εμφανίζουν κάποια συγκεκριμένα χαρακτηριστικά προσωπικότητας, όπως ευερεθιστότητα, ακαμψία, προσοχή, συμβατικότητα.
Διαφορική διάγνωση της νόσου Πάρκινσον
Όπως, προαναφέρθηκε, η διάγνωση της νόσου του Πάρκινσον είναι κλινική. Στην διαφορική διάγνωση της νόσου τίθεται μεγάλος αριθμός νοσημάτων, που εμπίπτουν σε μεγάλες κατηγορίες. Από αυτές ο κληρονομικός παρκινσονισμός, τα φαρμακευτικά αίτια παρκινσονισμού, τα εκφυλιστικά νοσήματα, ο αγγειακός παρκινσονισμός, τα τοξικά και τα λοιμώδη αίτια, αποτελούν τις κυριότερες, χωρίς να μπορεί να παραγνωριστεί η φυσιολογική γήρανση και ο ιδιοπαθής τρόμος.
Η φυσιολογική γήρανση είναι δύσκολο να ορισθεί, αλλά η βραδύτητα των κινήσεων, η σκυφτή στάση, η δυσκαμψία και η αστάθεια, είναι συνήθη στους ηλικιωμένους [65].
Ο ιδιοπαθής τρόμος χαρακτηρίζεται από τρόμο θέσης και κίνησης, συνήθως αμφοτερόπλευρο και τουλάχιστον στους μισούς ασθενείς, υπάρχει θετικό κληρονομικό.
Τα περισσότερα από τα νοσήματα που προκαλούν κληρονομικό παρκινσονισμό διακρίνονται εύκολα από την ιδιοπαθή νόσο του Πάρκινσον. Χαρακτηριστικά αναφέρονταιο αυτοσωμικά κυρίαρχος παρκινσονισμός που οφείλεται σε μεταλλάξεις στο γονίδιο της α-συνουκλεΐνης, οαυτοσωμικά υπολειπόμενος νεανικός παρκινσονισμός, που οφείλεταισε μεταλλάξεις στο γονίδιο της παρκίνης, ημετωποκροταφική άνοια με παρκινσονισμό κληρονομούμενη με το χρωμόσωμα 17, η νόσος του Huntington, όταν εκδηλώνεται σε ηλικία κάτω των 20 ετών , η νωτιοπαρεγκεφαλιδική αταξία τύπου 2 ή (SCA2,3).
Τα διάφορα φάρμακα αποτελούν αναστρέψιμη αιτία παρκινσονισμού, για την διάγνωση του οποίου απαιτείται λεπτομερές ιστορικό. Η συχνότερες αιτίες φαρμακευτικού παρκινσονισμού είναι τα αντιντοπαμινεργικά φάρμακα και οι αναστολείς διαύλων ασβεστίου. Τα υπόλοιπα προκαλούν παρκινσονισμό εξαιρετικά σπάνια και στα πλαίσια ιδιοσυγκρασικής αντίδρασης.
Τα εκφυλιστικά νοσήματα που πρέπει να διαφοροδιαγνωσθούν στην κλινική πράξη από την ιδιοπαθή νόσο του Πάρκινσον, είναι η προϊούσα υπερπυρηνική παράλυση (PSP) , η ατροφία πολλαπλών συστημάτων (MSA), η φλοιοβασική εκφύλιση (CBD) και η άνοια με σωμάτια Lewy (LBD).
Ο αγγειακός παρκινσονισμός[13] χαρακτηρίζεται από συμμετοχή κυρίως του κάτω μέρους του σώματος, με κύριο το συρτό βάδισμα, που είναι δυσανάλογα σοβαρότερο από τα άλλα σημεία παρκινσονισμού. Ανάλογος είναι και ο παρκινσονισμός του υδροκεφάλου [73], με συνοδό γνωστική έκπτωση και ακράτεια ούρων.
Από τις τοξίνες, το μαγγάνιο [74] προκαλεί επαγγελματική νόσο στους εργάτες μεταλλείων.
Από τα λοιμώδη και μεταλοιμώδη αίτια, σπάνια στην εποχή μας είναι η διάγνωση του μετεγκεφαλιτιδικούπαρκινσονισμού. Το ιστορικό εγκεφαλίτιδας με έντονη υπνηλία, η έναρξη σε νεαρή ηλικία, οι βολβοστροφικές κρίσεις, η οφθαλμοπληγία, οι διαταραχές συμπεριφοράς και ύπνου καθώς και η συνοδός εμφάνιση δυστονίας και τικς, συνηγορούν στην διάγνωση αυτή [75]. Η σοβαρότερη, ίσως αιτία ιογενούς παρκινσονισμού, στην εποχή μας είναι αυτή που προκαλεί ο ιός της ανθρώπινης ανοσοανεπάρκειας (HIV).
Η απεικόνιση στην νόσο του Πάρκινσον
Όπως έχει τονισθεί και νωρίτερα η διάγνωση της νόσου του Πάρκινσον είναι κλινική. Απεικονιστικές εξετάσεις συμβάλλουν κυρίως στην διαφορική διάγνωση άλλων νοσημάτων και συνδρόμων.
Η αξονική τομογραφία εγκεφάλου είναι καθοριστική για την διαφορική διάγνωση από την επασβέστωση βασικών γαγγλίων , και για την διαφορική διάγνωση από τον αγγειακό παρκινσονισμό και τον παρκινσονισμό του υδροκεφάλου.
Η μαγνητική τομογραφία εγκεφάλου ( MRI), παρότι δεν συμβάλλει ιδιαίτερα στην διάγνωση της νόσου Πάρκινσον είναι χρήσιμη στην διαφορική διάγνωσή της από άλλα εκφυλιστικά νοσήματα, όπως την MSA-P (ατροφία πολλαπλών συστημάτων με πρωτεύοντα τον παρκινσονισμό),την MSA-C (ατροφία πολλαπλών συστημάτων με πρωτεύουσα την παρεγκεφαλιδική διαταραχή) , την PSPκαι την CBD[79].
Το DATScan ή DopamineTransporterSPECT, αν και δεν επιτρέπει την αξιόπιστη διαφορική διάγνωση μεταξύ νόσου Πάρκινσον και MSA και PSP, είναι αξιόπιστο στην διάκριση της νόσου από τον ιδιοπαθή τρόμο [80], [81]. Επίσης, μπορεί να είναι χρήσιμο στην διαφοροδιάγνωση από τον αγγειακό παρκινσονισμό και τον φυσιολογικής τάσης υδροκέφαλο [80]. Τέλος, φαίνεται να είναι φυσιολογικό σε ασθενείς που παίρνουν νευροληπτικά και σε άλλες περιπτώσεις παρκινσονισμού χωρίς ραβδομέλαινα εκφύλιση, όπως στην δυστονία που απαντά στην ντόπα[82], ή στον ψυχογενή παρκινσονισμό[83].
Το διακρανιακό υπερηχογράφημα φαίνεται επίσης, χρήσιμο στην διαφορική διάγνωση της νόσου του Πάρκινσον.
Αιτιολογία της νόσου του Πάρκινσον
Είναι σχεδόν, καθολικά αποδεκτό, ότι ο συνδυασμός περιβαλλοντικών παραγόντων κινδύνου και γενετικής προδιάθεσης, οδηγεί τελικά στην παθογενετική αλληλουχία, με τελική κατάληξη την εμφάνιση της νόσου, χωρίς να είναι λίγοι ή λιγότερο φανατικοί με την άποψή τους, αυτοί που θεωρούν ότι το γενετικό μας υπόβαθρο είναι ικανό και αναγκαίο για να οδηγήσει στην νόσο.
Από τους μη γενετικούς παράγοντες κινδύνου τα μικροβιοκτόνα και παρασιτοκτόνα και ιδίως το παρακουάτ, και τoεθυλενοδιθειοκαρβαμίδιο του μαγγανίου, είναι πιθανό να δρουν συνεργικά αυξάνοντας τον κίνδυνο νόσου Πάρκινσον. Στον αντίποδα το κάπνισμα, έχει βρεθεί σε επιδημιολογικές μελέτες να έχει αρνητική συσχέτιση με την εμφάνιση νόσου, ενώ η καφεΐνη σχετίζεται αρνητικά με το κάπνισμα μόνον στους άντρες. Ως προς την κατανάλωση αλκοόλ, τα αποτελέσματα από κάποιες μελέτες δείχνουν αρνητική συσχέτιση, ενώ από άλλες μη στατιστικά σημαντική συσχέτιση. Επίσης, η χρήση μη στεροειδών αντιφλεγμονωδών σχετίζεται με χαμηλό κίνδυνο νόσου Πάρκινσον, γεγονός που μπορεί να δηλώνει τον νευροπροστατευτικό ρόλο τους , αν και απαιτούνται περαιτέρω μελέτες.
Η γενετική της νόσου του Πάρκινσον έλκει την μεγάλη μερίδα της έρευνας την δεκαετία που διανύουμε. Διακρίνουμε τα γονίδια που ευθύνονται για τις μονογενετικές μορφές της νόσου και τα γονίδια που σε συγκεκριμένους συνδυασμούς προδιαθέτουν για την σποραδική νόσο.
Οι μονογενετικές μορφές δεν έχουν ιδιαίτερο ρόλο στην σποραδική μορφή της νόσου και προκαλούν το 10% περίπου των περιπτώσεων της νόσου. Πολλές από αυτές φέρουν άτυπα χαρακτηριστικά, όπως πρώιμη έναρξη, δυστονία ή πρώιμη εμφάνιση άνοιας, ενώ άλλες είναι όμοιες με την σποραδική νόσο. Γονίδια που σχετίζονται με τις μορφές αυτές είναι: PARK 1 που κωδικοποιεί την α-συνουκλεḯνη, PARK2 που κωδικοποιεί την παρκίνη, PARK5 που κωδικοποιεί την UCHL1, PARK6 που κωδικοποιεί την PINK1, PARK5 που κωδικοποιεί την UCHL1, PARK7 που κωδικοποιεί την DJ-1, PARK8 που κωδικοποιεί την LRRK-2, PARK9 που κωδικοποιεί την ATP13A2, PARK13 που κωδικοποιεί την HTRA2.
Περίπου 10-15% των ασθενών με νόσο του Πάρκινσον φέρουν κληρονομικό ιστορικό συμβατό με αυτοσωμική κυρίαρχη ή υπολειπόμενη κληρονόμηση.
Πολλές μελέτες συσχέτισης έχουν γίνει σε υποψήφια γονίδια, που θεωρείται ότι συμβάλλουν στην αύξηση του κινδύνου για την εμφάνιση της σποραδικής νόσου. Τα πιο συχνά μελετώμενα γονίδια είναι αυτά που εμπλέκονται στον μεταβολισμό της ντοπαμίνης, στον μιτοχονδριακό μεταβολισμό, λιποπρωτεΐνες, ορμονικοί παράγοντες, παράγοντες που εμπλέκονται στον μεταβολισμό της ομοκυστεΐνης. Λίγοι από αυτούς τους πολυμορφισμούς (στα γονίδια NAT2, MAOB, GSTT1, το ε2 αλλήλιο της APOE ο H1 απλότυπος της tau), φάνηκε να σχετίζονται σημαντικά με την νόσο του Πάρκινσον, αλλά η παθοφυσιολογική τους σημασία είναι άγνωστη.
Παθογένεια της νόσου του Πάρκινσον
Με βάση την κλασική θεώρηση της παθογένειας της νόσου του Πάρκινσον, το οξειδωτικό στρες, η μιτοχονδριακή δυσλειτουργία, η φλεγμονή και η διεγερτοτοξικότητα του γλουταμικού, οδηγούν στον θάνατο των ντοπαμινεργικών νευρώνων μέσω απόπτωσης. Πλέον, γνωρίζουμε ότι τον καθοριστικότερο ρόλο στην εκφυλιστική διεργασία τον έχει το πρωτεολυτικό στρες, που προκύπτει από την δυσλειτουργία του συστήματος ουμπικουιτίνης – πρωτεοσώματος. Αυτό έγινε φανερό μετά την ανακάλυψη των μεταλλάξεων που οδηγούν στις κληρονομικές μορφές της νόσου ή οδηγούν σε προδιάθεση για την σποραδική μορφή.
Φαίνεται, ότι ο παθογενετικός μηχανισμός που οδηγεί στην νόσο του Πάρκινσον είναι πολύπλοκος και ποικιλία παραγόντων αλληλεπιδρούν μεταξύ τους. Παράγοντες που προκαλλούν οξειδωτικό στρες μπορούν να οδηγήσουν σε μιτοχονδριακή βλάβη και δυσλειτουργία του πρωτεοσώματος, και αντίστροφα η μιτοχονδριακή δυσλειτουργία μπορεί να οδηγήσει σε οξειδωτικό στρες και δυσλειτουργία του πρωτεοσώματος. Παρόμοια, η αναστολή της λειτουργίας του πρωτεοσώματος, θα μπορούσε να οδηγήσει σε οξειδωτικό στρες, μιτοχονδριακή δυσλειτουργία , φλεγμονώδη αντίδραση , και απόπτωση . Επιπλέον, συνδυασμός παραγόντων, όπως το οξειδωτικό στρες και η αναστολή της λειτουργίας του προτεοσώματος, μπορούν να οδηγήσουν συνεργικά, σε παθολογική αναδίπλωση πρωτεινών.
Θεραπεία της νόσου Πάρκινσον
Ίσως το πιο επαναστατικό βήμα στην αντιμετώπιση της νόσου του Πάρκινσον έγινε το 1967, όταν ο Κοτζιάς[95], εισήγαγε την λεβοντόπα, για πρώτη φορά σε μεγάλες δόσεις. Ίσως η σημαντικότερη πρόοδος που έχει γίνει έκτοτε, είναι η αποδοχή ότι τα κινητικά συμπτώματα της νόσου δεν είναι ο μόνος στόχος. Τα μη κινητικά συμπτώματα και οι επιπλοκές κινητικές και μη της νόσου και της θεραπείας (πίνακας) επηρεάζουν το ίδιο, αν όχι περισσότερο την ποιότητα ζωής των ασθενών . Άλλωστε, η καθυστέρηση ή /και ανακοπή της εξέλιξης της νόσου (νευροπροστασία), αποτελεί το κύριο μέλημα της έρευνας στις μέρες μας.
Η L-dopa συνεχίζει να αποτελεί το πιο αποτελεσματικό διαθέσιμο φάρμακο για την ανακούφιση των κινητικών συμπτωμάτων της νόσου, της βραδυκινησίας, της δυσκαμψίας και του τρόμου. Ο κίνδυνος ωστόσο της πρώιμης εμφάνισης κινητικών επιπλοκών καθυστερεί την εισαγωγή της στην θεραπεία.
Φάρμακα που ενισχύουν την δράση της λεβοντόπα μειώνοντας την αποδόμησή της είναι οι αναστολείς της COMT, εντακαπόνη και τολκαπόνη. Επίσης, οι αναστολείς της ΜΑΟ-Β, εμποδίζουν την οξειδωτική απαμίνωση της ντοπαμίνης και αυξάνουν την ημιπερίοδο ζωής της στον εγκέφαλο. Δύο αναστολείς της ΜΑΟ-Β βρίσκονται αυτήν την στιγμή σε κυκλοφορία, η σελεγιλίνη και η ρασαγιλίνη. Πρόσφατες μελέτες, έδωσαν ενδείξεις ότι η ρασαγιλίνη μπορεί να τροποποιεί την πορεία της νόσου, ιδιαίτερα αν χορηγηθεί πρώιμα.
Τα αντιχολινεργικά, έχουν παραγκωνισθεί στις μέρες μας εξαιτίας της ανησυχίας για τα αποτελέσματά τους στην πρόσφατη μνήμη, τις ψευδαισθήσεις την επίσχεση κοπράνων και ούρων. Παρόλα μπορεί να είναι χρήσιμα σε νέους ασθενείς με δυστονία ή με σοβαρό τρόμο ηρεμίας.
Οι αγωνιστές ντοπαμίνης δίνουν την δυνατότητα να καθυστερούμε την έναρξη της λεβοντόπαή να μειώνουμε την δόση της αλλά και να μειώνουμε τις κινητικές επιπλοκές της νόσου, αυξάνοντας τον χρόνο off.
Η περγολίδη και η καμπεργολίνη έχουν τα παραπάνω πλεονεκτήματα, η χρήση τους, όμως, έχει περιοριστεί λόγω του κινδύνου ανάπτυξης οπισθοπεριτοναικήςίνωσης και βαλβιδοπάθειας. Η ροπινιρόλη και η πραμιπεξόλη έχουν όλα τα πλεονεκτήματα των αγωνιστών ντοπαμίνης, χωρίς τους παραπάνω κινδύνους, αλλά με συχνή εμφάνιση υπνηλίας.
Η ροτιγοτίνη είναι ο αγωνιστής υποδοχέων ντοπαμίνης με διαδερμική χορήγηση, που παρακάμπτει το γαστρεντερικό και ίσως διευκολύνει τη συμμόρφωση των ασθενών. Η απομορφίνη χορηγείται παρεντερικά (υποδόρια), είτε σαν θεραπεία «διάσωσης» στα απρόβλεπτα offsκαι τα παγώματα, είτε ως αντλία απομορφίνης η οποία δίνοντας την δυνατότητα συνεχούς χορήγησης μειώνει τις υπερκινησίες, αυξάνοντας τον χρόνο “on”.
Η αμανταδίνη με πολλαπλό μηχανισμό δράσης, χρησιμοποιείται, πλέον, κυρίως στην αντιμετώπιση των υπερκινησιών στα προχωρημένα στάδια.
Σε ασθενείς που πληρούν συγκεκριμένα κριτήρια, προτείνεται η χειρουργική αντιμετώπιση της νόσου του Πάρκινσον.
Οι ενδείξεις της είναι [150]:
Η εν τω βάθει εγκεφαλική διέγερση του υποθαλαμίου πυρήνα (STNDBS) αποτελεί την εξέλιξη των θαλαμοτομών και ωχροτομών, και έχει παρόμοια αποτελέσματα με την λεβοντόπα στην αντιμετώπιση των κινητικών συμπτωμάτων, με εντυπωσιακά ταυτόχρονα αποτελέσματα στην αντιμετώπιση των κινητικών επιπλοκών.
Απαραίτητη είναι βέβαια η σωστή επιλογή των ασθενών, ενώ είναι σημαντικό να γνωρίζει ο ασθενής τι πρέπει να περιμένει. Συμπτώματα που δεν απαντούν στην ντοπαμίνη (διαταραχές ομιλίας, δυσφαγία, διαταραχές ύπνου, παγώματα, διαταραχές του αυτονόμου), δεν απαντούν και στην λειτουργική χειρουργική. Ως επεμβατική μέθοδος έχει επίσης ανεπιθύμητες ενέργειες, που, αν και σπάνιες, είναι ενδεχόμενες (ενδοεγκεφαλική αιμορραγία, ψυχιατρικά, επιπλοκές χειρουργείου).
Άλλες θεραπευτικές επίλογές, που βρίσκονται υπό μελέτη είναι η μεταμόσχευση ανθρώπινων μελανινωμένων επιθηλιακών κυττάρων, διάφοροι αναστολείς της απόπτωσης, η διαγονιδιακή έκφραση GDNF, συνδυασμένες θεραπείες αντιαποπτωτικών παραγόντων και GDNF, διαγονιδιακή προσθήκη ενζύμων που εμπλέκονται στην βιοσύνθεση της ντοπαμίνης, stemcells που διαφοροποιούνται σε λειτουργικά ντοπαμινεργικά κύτταρα με γενετική τροποποίηση και διαγονιδιακή παραγωγή GABA στον STN, το CoQ10, η κρεατίνη, ημινοκυκλίνη, κτλ.
Στις βιομηχανοποιημένες χώρες 0,3%, του γενικού πληθυσμού και 1% των ατόμων άνω των 60 ετών πάσχουν από νόσο Πάρκινσον [18]. Είναι λιγότερο συχνή σε μαύρους και ασιάτες από ότι στους λευκούς και οι μάλλον, συχνότερη στους άντρες [25], [24], [22], ίσως λόγω της προστατευτικής δράσης των οιστρογόνων στις στις γυναίκες .
Η έναρξη της νόσου είναι σπάνια σε ηλικίες κάτω των 50 και υπάρχει σχεδόν κάθετη αύξηση μετά τα 60.
Διάγνωση της νόσου του Πάρκινσον
Η διάγνωση της νόσου του Πάρκινσον είναι κατά βάση κλινική, ενώ εργαστηριακές εξετάσεις μπορεί να απαιτούνται για να αποκλείσουν νοσήματα που μιμούνται την νόσο.
Τα θεμελιώδη χαρακτηριστικά της νόσου είναι η βραδυκινησία, ο τρόμος ηρεμίας και η δυσκαμψία, ενώ η αστάθεια είναι μη ειδική και σπάνια εμφανίζεται στην έναρξη της νόσου.
Η βραδυκινησία είναι, ίσως το πιο ενοχλητικό σύμπτωμα της πρώιμης νόσου. Εκδηλώνεται αρχικά με δυσκολία στις λεπτές κινήσεις, όπως το κούμπωμα των κουμπιών ή το γράψιμο και με την μείωση των αιωρήσεων των άκρων στην βάδιση.
Ο τρόμος ηρεμίας(τρέμουλο) με συχνότητα τυπικά 4-6 Hz (τρόμος καταμέτρησης καταποτίων ή κερμάτων, “pillrolling”) έχει συνήθως ασύμμετρη έναρξη και χειροτερεύει με το άγχος, την ετερόπλευρη κινητική δραστηριότητα και κατά την βάδιση.
Η δυσκαμψία είναι η συνεχής και ομοιόμορφη αύξηση του μυϊκού τόνου.
Η αστάθεια αναφέρεται στην σταδιακή ανάπτυξη διαταραχής ισορροπίας, που οδηγεί σε αυξημένο κίνδυνο πτώσεων.
Ο ασθενής συνήθως αντιλαμβάνεται την έναρξη της νόσου, ως δυσκολία στις λεπτές κινήσεις, όπως στο κούμπωμα ή το ξύρισμα, ένα ήπιο τρέμουλο σε ένα χέρι και υποκειμενική (αρχικά) αστάθεια στην βάδιση.
Πολύ νωρίτερα, εμφανίζονται συμπτώματα που είναιπροκλινικά χαρακτηριστικά της νόσου και παλαιότερα θεωρούνταν «παράγοντες κινδύνου» για την ανάπτυξη της νόσου.
Τα πλέον πρώιμα από αυτά είναι η δυσκοιλιότητα και η διαταραχή της όσφρησης. Ακολουθούν, οι διαταραχές του ύπνου, διάφορα σύνδρομα πόνου, όπως κεφαλαλγίες, άγχος, διαταραχή πανικού, μειωμένη ικανότητα διαχείρισης του άγχους, συναισθηματικές διαταραχές, βραδύτητα σκέψης, κατάθλιψη, κόπωση, παροδικά κινητικά συμπτώματα και γνωστικά ελλείμματα.
Παρότι δεν υπάρχουν μεγάλες προοπτικές μελέτες που να το αποδεικνύουν, φαίνεται ότι οι ασθενείς με πρώιμη ή υποκλινική νόσο εμφανίζουν κάποια συγκεκριμένα χαρακτηριστικά προσωπικότητας, όπως ευερεθιστότητα, ακαμψία, προσοχή, συμβατικότητα.
Διαφορική διάγνωση της νόσου Πάρκινσον
Όπως, προαναφέρθηκε, η διάγνωση της νόσου του Πάρκινσον είναι κλινική. Στην διαφορική διάγνωση της νόσου τίθεται μεγάλος αριθμός νοσημάτων, που εμπίπτουν σε μεγάλες κατηγορίες. Από αυτές ο κληρονομικός παρκινσονισμός, τα φαρμακευτικά αίτια παρκινσονισμού, τα εκφυλιστικά νοσήματα, ο αγγειακός παρκινσονισμός, τα τοξικά και τα λοιμώδη αίτια, αποτελούν τις κυριότερες, χωρίς να μπορεί να παραγνωριστεί η φυσιολογική γήρανση και ο ιδιοπαθής τρόμος.
Η φυσιολογική γήρανση είναι δύσκολο να ορισθεί, αλλά η βραδύτητα των κινήσεων, η σκυφτή στάση, η δυσκαμψία και η αστάθεια, είναι συνήθη στους ηλικιωμένους [65].
Ο ιδιοπαθής τρόμος χαρακτηρίζεται από τρόμο θέσης και κίνησης, συνήθως αμφοτερόπλευρο και τουλάχιστον στους μισούς ασθενείς, υπάρχει θετικό κληρονομικό.
Τα περισσότερα από τα νοσήματα που προκαλούν κληρονομικό παρκινσονισμό διακρίνονται εύκολα από την ιδιοπαθή νόσο του Πάρκινσον. Χαρακτηριστικά αναφέρονταιο αυτοσωμικά κυρίαρχος παρκινσονισμός που οφείλεται σε μεταλλάξεις στο γονίδιο της α-συνουκλεΐνης, οαυτοσωμικά υπολειπόμενος νεανικός παρκινσονισμός, που οφείλεταισε μεταλλάξεις στο γονίδιο της παρκίνης, ημετωποκροταφική άνοια με παρκινσονισμό κληρονομούμενη με το χρωμόσωμα 17, η νόσος του Huntington, όταν εκδηλώνεται σε ηλικία κάτω των 20 ετών , η νωτιοπαρεγκεφαλιδική αταξία τύπου 2 ή (SCA2,3).
Τα διάφορα φάρμακα αποτελούν αναστρέψιμη αιτία παρκινσονισμού, για την διάγνωση του οποίου απαιτείται λεπτομερές ιστορικό. Η συχνότερες αιτίες φαρμακευτικού παρκινσονισμού είναι τα αντιντοπαμινεργικά φάρμακα και οι αναστολείς διαύλων ασβεστίου. Τα υπόλοιπα προκαλούν παρκινσονισμό εξαιρετικά σπάνια και στα πλαίσια ιδιοσυγκρασικής αντίδρασης.
Τα εκφυλιστικά νοσήματα που πρέπει να διαφοροδιαγνωσθούν στην κλινική πράξη από την ιδιοπαθή νόσο του Πάρκινσον, είναι η προϊούσα υπερπυρηνική παράλυση (PSP) , η ατροφία πολλαπλών συστημάτων (MSA), η φλοιοβασική εκφύλιση (CBD) και η άνοια με σωμάτια Lewy (LBD).
Ο αγγειακός παρκινσονισμός[13] χαρακτηρίζεται από συμμετοχή κυρίως του κάτω μέρους του σώματος, με κύριο το συρτό βάδισμα, που είναι δυσανάλογα σοβαρότερο από τα άλλα σημεία παρκινσονισμού. Ανάλογος είναι και ο παρκινσονισμός του υδροκεφάλου [73], με συνοδό γνωστική έκπτωση και ακράτεια ούρων.
Από τις τοξίνες, το μαγγάνιο [74] προκαλεί επαγγελματική νόσο στους εργάτες μεταλλείων.
Από τα λοιμώδη και μεταλοιμώδη αίτια, σπάνια στην εποχή μας είναι η διάγνωση του μετεγκεφαλιτιδικούπαρκινσονισμού. Το ιστορικό εγκεφαλίτιδας με έντονη υπνηλία, η έναρξη σε νεαρή ηλικία, οι βολβοστροφικές κρίσεις, η οφθαλμοπληγία, οι διαταραχές συμπεριφοράς και ύπνου καθώς και η συνοδός εμφάνιση δυστονίας και τικς, συνηγορούν στην διάγνωση αυτή [75]. Η σοβαρότερη, ίσως αιτία ιογενούς παρκινσονισμού, στην εποχή μας είναι αυτή που προκαλεί ο ιός της ανθρώπινης ανοσοανεπάρκειας (HIV).
Η απεικόνιση στην νόσο του Πάρκινσον
Όπως έχει τονισθεί και νωρίτερα η διάγνωση της νόσου του Πάρκινσον είναι κλινική. Απεικονιστικές εξετάσεις συμβάλλουν κυρίως στην διαφορική διάγνωση άλλων νοσημάτων και συνδρόμων.
Η αξονική τομογραφία εγκεφάλου είναι καθοριστική για την διαφορική διάγνωση από την επασβέστωση βασικών γαγγλίων , και για την διαφορική διάγνωση από τον αγγειακό παρκινσονισμό και τον παρκινσονισμό του υδροκεφάλου.
Η μαγνητική τομογραφία εγκεφάλου ( MRI), παρότι δεν συμβάλλει ιδιαίτερα στην διάγνωση της νόσου Πάρκινσον είναι χρήσιμη στην διαφορική διάγνωσή της από άλλα εκφυλιστικά νοσήματα, όπως την MSA-P (ατροφία πολλαπλών συστημάτων με πρωτεύοντα τον παρκινσονισμό),την MSA-C (ατροφία πολλαπλών συστημάτων με πρωτεύουσα την παρεγκεφαλιδική διαταραχή) , την PSPκαι την CBD[79].
Το DATScan ή DopamineTransporterSPECT, αν και δεν επιτρέπει την αξιόπιστη διαφορική διάγνωση μεταξύ νόσου Πάρκινσον και MSA και PSP, είναι αξιόπιστο στην διάκριση της νόσου από τον ιδιοπαθή τρόμο [80], [81]. Επίσης, μπορεί να είναι χρήσιμο στην διαφοροδιάγνωση από τον αγγειακό παρκινσονισμό και τον φυσιολογικής τάσης υδροκέφαλο [80]. Τέλος, φαίνεται να είναι φυσιολογικό σε ασθενείς που παίρνουν νευροληπτικά και σε άλλες περιπτώσεις παρκινσονισμού χωρίς ραβδομέλαινα εκφύλιση, όπως στην δυστονία που απαντά στην ντόπα[82], ή στον ψυχογενή παρκινσονισμό[83].
Το διακρανιακό υπερηχογράφημα φαίνεται επίσης, χρήσιμο στην διαφορική διάγνωση της νόσου του Πάρκινσον.
Αιτιολογία της νόσου του Πάρκινσον
Είναι σχεδόν, καθολικά αποδεκτό, ότι ο συνδυασμός περιβαλλοντικών παραγόντων κινδύνου και γενετικής προδιάθεσης, οδηγεί τελικά στην παθογενετική αλληλουχία, με τελική κατάληξη την εμφάνιση της νόσου, χωρίς να είναι λίγοι ή λιγότερο φανατικοί με την άποψή τους, αυτοί που θεωρούν ότι το γενετικό μας υπόβαθρο είναι ικανό και αναγκαίο για να οδηγήσει στην νόσο.
Από τους μη γενετικούς παράγοντες κινδύνου τα μικροβιοκτόνα και παρασιτοκτόνα και ιδίως το παρακουάτ, και τoεθυλενοδιθειοκαρβαμίδιο του μαγγανίου, είναι πιθανό να δρουν συνεργικά αυξάνοντας τον κίνδυνο νόσου Πάρκινσον. Στον αντίποδα το κάπνισμα, έχει βρεθεί σε επιδημιολογικές μελέτες να έχει αρνητική συσχέτιση με την εμφάνιση νόσου, ενώ η καφεΐνη σχετίζεται αρνητικά με το κάπνισμα μόνον στους άντρες. Ως προς την κατανάλωση αλκοόλ, τα αποτελέσματα από κάποιες μελέτες δείχνουν αρνητική συσχέτιση, ενώ από άλλες μη στατιστικά σημαντική συσχέτιση. Επίσης, η χρήση μη στεροειδών αντιφλεγμονωδών σχετίζεται με χαμηλό κίνδυνο νόσου Πάρκινσον, γεγονός που μπορεί να δηλώνει τον νευροπροστατευτικό ρόλο τους , αν και απαιτούνται περαιτέρω μελέτες.
Η γενετική της νόσου του Πάρκινσον έλκει την μεγάλη μερίδα της έρευνας την δεκαετία που διανύουμε. Διακρίνουμε τα γονίδια που ευθύνονται για τις μονογενετικές μορφές της νόσου και τα γονίδια που σε συγκεκριμένους συνδυασμούς προδιαθέτουν για την σποραδική νόσο.
Οι μονογενετικές μορφές δεν έχουν ιδιαίτερο ρόλο στην σποραδική μορφή της νόσου και προκαλούν το 10% περίπου των περιπτώσεων της νόσου. Πολλές από αυτές φέρουν άτυπα χαρακτηριστικά, όπως πρώιμη έναρξη, δυστονία ή πρώιμη εμφάνιση άνοιας, ενώ άλλες είναι όμοιες με την σποραδική νόσο. Γονίδια που σχετίζονται με τις μορφές αυτές είναι: PARK 1 που κωδικοποιεί την α-συνουκλεḯνη, PARK2 που κωδικοποιεί την παρκίνη, PARK5 που κωδικοποιεί την UCHL1, PARK6 που κωδικοποιεί την PINK1, PARK5 που κωδικοποιεί την UCHL1, PARK7 που κωδικοποιεί την DJ-1, PARK8 που κωδικοποιεί την LRRK-2, PARK9 που κωδικοποιεί την ATP13A2, PARK13 που κωδικοποιεί την HTRA2.
Περίπου 10-15% των ασθενών με νόσο του Πάρκινσον φέρουν κληρονομικό ιστορικό συμβατό με αυτοσωμική κυρίαρχη ή υπολειπόμενη κληρονόμηση.
Πολλές μελέτες συσχέτισης έχουν γίνει σε υποψήφια γονίδια, που θεωρείται ότι συμβάλλουν στην αύξηση του κινδύνου για την εμφάνιση της σποραδικής νόσου. Τα πιο συχνά μελετώμενα γονίδια είναι αυτά που εμπλέκονται στον μεταβολισμό της ντοπαμίνης, στον μιτοχονδριακό μεταβολισμό, λιποπρωτεΐνες, ορμονικοί παράγοντες, παράγοντες που εμπλέκονται στον μεταβολισμό της ομοκυστεΐνης. Λίγοι από αυτούς τους πολυμορφισμούς (στα γονίδια NAT2, MAOB, GSTT1, το ε2 αλλήλιο της APOE ο H1 απλότυπος της tau), φάνηκε να σχετίζονται σημαντικά με την νόσο του Πάρκινσον, αλλά η παθοφυσιολογική τους σημασία είναι άγνωστη.
Παθογένεια της νόσου του Πάρκινσον
Με βάση την κλασική θεώρηση της παθογένειας της νόσου του Πάρκινσον, το οξειδωτικό στρες, η μιτοχονδριακή δυσλειτουργία, η φλεγμονή και η διεγερτοτοξικότητα του γλουταμικού, οδηγούν στον θάνατο των ντοπαμινεργικών νευρώνων μέσω απόπτωσης. Πλέον, γνωρίζουμε ότι τον καθοριστικότερο ρόλο στην εκφυλιστική διεργασία τον έχει το πρωτεολυτικό στρες, που προκύπτει από την δυσλειτουργία του συστήματος ουμπικουιτίνης – πρωτεοσώματος. Αυτό έγινε φανερό μετά την ανακάλυψη των μεταλλάξεων που οδηγούν στις κληρονομικές μορφές της νόσου ή οδηγούν σε προδιάθεση για την σποραδική μορφή.
Φαίνεται, ότι ο παθογενετικός μηχανισμός που οδηγεί στην νόσο του Πάρκινσον είναι πολύπλοκος και ποικιλία παραγόντων αλληλεπιδρούν μεταξύ τους. Παράγοντες που προκαλλούν οξειδωτικό στρες μπορούν να οδηγήσουν σε μιτοχονδριακή βλάβη και δυσλειτουργία του πρωτεοσώματος, και αντίστροφα η μιτοχονδριακή δυσλειτουργία μπορεί να οδηγήσει σε οξειδωτικό στρες και δυσλειτουργία του πρωτεοσώματος. Παρόμοια, η αναστολή της λειτουργίας του πρωτεοσώματος, θα μπορούσε να οδηγήσει σε οξειδωτικό στρες, μιτοχονδριακή δυσλειτουργία , φλεγμονώδη αντίδραση , και απόπτωση . Επιπλέον, συνδυασμός παραγόντων, όπως το οξειδωτικό στρες και η αναστολή της λειτουργίας του προτεοσώματος, μπορούν να οδηγήσουν συνεργικά, σε παθολογική αναδίπλωση πρωτεινών.
Θεραπεία της νόσου Πάρκινσον
Ίσως το πιο επαναστατικό βήμα στην αντιμετώπιση της νόσου του Πάρκινσον έγινε το 1967, όταν ο Κοτζιάς[95], εισήγαγε την λεβοντόπα, για πρώτη φορά σε μεγάλες δόσεις. Ίσως η σημαντικότερη πρόοδος που έχει γίνει έκτοτε, είναι η αποδοχή ότι τα κινητικά συμπτώματα της νόσου δεν είναι ο μόνος στόχος. Τα μη κινητικά συμπτώματα και οι επιπλοκές κινητικές και μη της νόσου και της θεραπείας (πίνακας) επηρεάζουν το ίδιο, αν όχι περισσότερο την ποιότητα ζωής των ασθενών . Άλλωστε, η καθυστέρηση ή /και ανακοπή της εξέλιξης της νόσου (νευροπροστασία), αποτελεί το κύριο μέλημα της έρευνας στις μέρες μας.
Η L-dopa συνεχίζει να αποτελεί το πιο αποτελεσματικό διαθέσιμο φάρμακο για την ανακούφιση των κινητικών συμπτωμάτων της νόσου, της βραδυκινησίας, της δυσκαμψίας και του τρόμου. Ο κίνδυνος ωστόσο της πρώιμης εμφάνισης κινητικών επιπλοκών καθυστερεί την εισαγωγή της στην θεραπεία.
Φάρμακα που ενισχύουν την δράση της λεβοντόπα μειώνοντας την αποδόμησή της είναι οι αναστολείς της COMT, εντακαπόνη και τολκαπόνη. Επίσης, οι αναστολείς της ΜΑΟ-Β, εμποδίζουν την οξειδωτική απαμίνωση της ντοπαμίνης και αυξάνουν την ημιπερίοδο ζωής της στον εγκέφαλο. Δύο αναστολείς της ΜΑΟ-Β βρίσκονται αυτήν την στιγμή σε κυκλοφορία, η σελεγιλίνη και η ρασαγιλίνη. Πρόσφατες μελέτες, έδωσαν ενδείξεις ότι η ρασαγιλίνη μπορεί να τροποποιεί την πορεία της νόσου, ιδιαίτερα αν χορηγηθεί πρώιμα.
Τα αντιχολινεργικά, έχουν παραγκωνισθεί στις μέρες μας εξαιτίας της ανησυχίας για τα αποτελέσματά τους στην πρόσφατη μνήμη, τις ψευδαισθήσεις την επίσχεση κοπράνων και ούρων. Παρόλα μπορεί να είναι χρήσιμα σε νέους ασθενείς με δυστονία ή με σοβαρό τρόμο ηρεμίας.
Οι αγωνιστές ντοπαμίνης δίνουν την δυνατότητα να καθυστερούμε την έναρξη της λεβοντόπαή να μειώνουμε την δόση της αλλά και να μειώνουμε τις κινητικές επιπλοκές της νόσου, αυξάνοντας τον χρόνο off.
Η περγολίδη και η καμπεργολίνη έχουν τα παραπάνω πλεονεκτήματα, η χρήση τους, όμως, έχει περιοριστεί λόγω του κινδύνου ανάπτυξης οπισθοπεριτοναικήςίνωσης και βαλβιδοπάθειας. Η ροπινιρόλη και η πραμιπεξόλη έχουν όλα τα πλεονεκτήματα των αγωνιστών ντοπαμίνης, χωρίς τους παραπάνω κινδύνους, αλλά με συχνή εμφάνιση υπνηλίας.
Η ροτιγοτίνη είναι ο αγωνιστής υποδοχέων ντοπαμίνης με διαδερμική χορήγηση, που παρακάμπτει το γαστρεντερικό και ίσως διευκολύνει τη συμμόρφωση των ασθενών. Η απομορφίνη χορηγείται παρεντερικά (υποδόρια), είτε σαν θεραπεία «διάσωσης» στα απρόβλεπτα offsκαι τα παγώματα, είτε ως αντλία απομορφίνης η οποία δίνοντας την δυνατότητα συνεχούς χορήγησης μειώνει τις υπερκινησίες, αυξάνοντας τον χρόνο “on”.
Η αμανταδίνη με πολλαπλό μηχανισμό δράσης, χρησιμοποιείται, πλέον, κυρίως στην αντιμετώπιση των υπερκινησιών στα προχωρημένα στάδια.
Σε ασθενείς που πληρούν συγκεκριμένα κριτήρια, προτείνεται η χειρουργική αντιμετώπιση της νόσου του Πάρκινσον.
Οι ενδείξεις της είναι [150]:
- Σοβαρές κινητικές διακυμάνσεις και υπερκινησίες, παρά την χορήγηση της καλύτερης δυνατής φαρμακευτικής αγωγής
- Μη ανοχή ή ανεπιθύμητες ενέργειες προκαλούμενες από την φαρμακευτική αγωγή, χωρίς ικανοποιητικό έλεγχο των συμπτωμάτων
- Τρόμος που οδηγεί σε ανικανότητα, ανθεκτικός στην φαρμακευτική αγωγή.
Η εν τω βάθει εγκεφαλική διέγερση του υποθαλαμίου πυρήνα (STNDBS) αποτελεί την εξέλιξη των θαλαμοτομών και ωχροτομών, και έχει παρόμοια αποτελέσματα με την λεβοντόπα στην αντιμετώπιση των κινητικών συμπτωμάτων, με εντυπωσιακά ταυτόχρονα αποτελέσματα στην αντιμετώπιση των κινητικών επιπλοκών.
Απαραίτητη είναι βέβαια η σωστή επιλογή των ασθενών, ενώ είναι σημαντικό να γνωρίζει ο ασθενής τι πρέπει να περιμένει. Συμπτώματα που δεν απαντούν στην ντοπαμίνη (διαταραχές ομιλίας, δυσφαγία, διαταραχές ύπνου, παγώματα, διαταραχές του αυτονόμου), δεν απαντούν και στην λειτουργική χειρουργική. Ως επεμβατική μέθοδος έχει επίσης ανεπιθύμητες ενέργειες, που, αν και σπάνιες, είναι ενδεχόμενες (ενδοεγκεφαλική αιμορραγία, ψυχιατρικά, επιπλοκές χειρουργείου).
Άλλες θεραπευτικές επίλογές, που βρίσκονται υπό μελέτη είναι η μεταμόσχευση ανθρώπινων μελανινωμένων επιθηλιακών κυττάρων, διάφοροι αναστολείς της απόπτωσης, η διαγονιδιακή έκφραση GDNF, συνδυασμένες θεραπείες αντιαποπτωτικών παραγόντων και GDNF, διαγονιδιακή προσθήκη ενζύμων που εμπλέκονται στην βιοσύνθεση της ντοπαμίνης, stemcells που διαφοροποιούνται σε λειτουργικά ντοπαμινεργικά κύτταρα με γενετική τροποποίηση και διαγονιδιακή παραγωγή GABA στον STN, το CoQ10, η κρεατίνη, ημινοκυκλίνη, κτλ.
►
▼
Δυστονία
Η δυστονία ορίζεται ως το νευρολογικό σύνδρομο, που χαρακτηρίζεται από ακούσιες, παρατεταμένες, σταθερές ως προς τη μορφή τους και συχνά επαναλαμβανόμενες μυϊκές συσπάσεις αντιθετικών μυών, που προκαλούν ανώμαλες / αφύσικες θέσεις ή στάσεις.
Χαρακτηριστική είναι η διατήρηση συγκεκριμένου μοτίβου κινήσεων, ανεξάρτητα αν αυτές είναι αργές ή πιο γρήγορες.
Συχνά η δυστονία συνοδεύεται από τρόμο (τρέμουλο), που μπορεί να αφορά την περιοχή του σώματος που πάσχει ή άλλες περιοχές π.χ μπορεί να έχουμε τρόμο χειρών σε αυχενική δυστονία.
Υπάρχουν πολλά είδη δυστονίας: μπορεί να είναι συνεχής ή με διακυμάνσεις, πρωτοπαθής ή δευτεροπαθής, κληρονομική ή σποραδική, να εμφανίζεται σε παιδική ηλικία ή μετά την ενηλικίωση, να εμφανίζεται σε κίνηση ή σε ηρεμία, να είναι περιορισμένη σε ένα μέρος του σώματος ή να είναι γενικευμένη.
Ίσως οι συχνότερες μορφές δυστονίας είναι οι σποραδικές, εστιακές δυστονίες. Η αυχενική δυστονία ή σπασμωδικό ραιβόκρανο (εικ 1) εμφανίζεται κατά τι συχνότερα σε γυναίκες, μέσης ηλικίας. Συνήθως, εμφανίζεται με κάμψη και στροφή της κεφαλής προς μία πλευρά, ενίοτε με ανύψωση του σύστοιχου ώμου και στροφή του πηγουνιού προς αυτόν. Μπορεί να συνοδεύεται από κάμψη της κεφαλής προς τα πίσω ή προς τα εμπρός. Σπάνια η κεφαλή μπορεί να πάρει μια σταθερή θέση, συνήθως οι συσπάσεις των μυών του αυχένα προκαλούν τρομώδη κίνηση της κεφαλής. Σε λιγότερο από 10% των ασθενών μπορεί να υπάρξει αυτόματη ύφεση των συμπτωμάτων μέσα στα πρώτα τρία χρόνια, στους περισσότερους, όμως, ασθενείς μπορεί να διαρκέσει εφ’ όρου ζωής. Η αιτιολογία δεν είναι γνωστή, αν και υπάρχουν πολλές θεωρίες που εμπλέκουν διαταραχές στην προσαγωγή αιθουσαίων ερεθισμάτων, γενετικούς παράγοντες, περιφερικό τραύμα κτλ. Μέχρι σήμερα, η καλύτερη αντιμετώπιση της κατάστασης είναι με ενέσεις αλλαντικής τοξίνης (Bot. Tox), από εξειδικευμένο στις διαταραχές κινητικότητας νευρολόγο.
Ο βλεφαρόσπασμος, μια άλλη μορφή εστιακής δυστονίας, χαρακτηρίζεται από σπασμωδικές συσπάσεις του σφικτήρα των βλεφάρων, που μπορεί να συνοδεύεται από συσπάσεις και άλλων μυών του προσώπου ή του στόματος.
Συνήθως, επιδεινώνεται με το δυνατό φως, τον αέρα, τις κινήσεις και το στρες. Μπορεί να οδηγήσει σε προβλήματα στην καθημερινή ζωή, αφού μπορεί να οδηγήσει, ακόμα και σε δυσκολία του ασθενή να διασχίσει το δρόμο. Ο πρωτοεμφανιζόμενος βλεφαρόσπασμος, πρέπει να διαφοροδιαγνωσθεί από άλλες καταστάσεις, που μπορεί να προκαλούν πτώση βλεφάρου, καθώς και από δευτεροπαθή βλεφαρόσπασμο, που μπορεί να οφείλεται σε δομικές βλάβες. Ο θεράπων νευρολόγος, κρίνει και αποφασίζει την διενέργεια μαγνητικής τομογραφίας εγκεφάλου για αποκλεισμό τέτοιων βλαβών. Η αντιμετώπιση είναι και σε αυτήν την εστιακή δυστονία με ενέσεις αλλαντικής τοξίνης (Bot. Tox), από εξειδικευμένο στις διαταραχές κινητικότητας νευρολόγο.
Ιδιαίτερη κατηγορία εστιακής δυστονίας είναι η σχετιζόμενη με την πράξη, όπως η δυστονία γραφέως και άλλες επαγγελματικές δυστονίες, όπως η δυστονία των μουσικών. Αυτές εμφανίζονται σε ασθενείς, που χρησιμοποιούν υπερεντατικά το προσβεβλημένο μέλος, για συγκεκριμένη δραστηριότητα, όπως γραφή ή τη χρήση μουσικών οργάνων.
Η δυστονία αφορά μόνο στη συγκεκριμένη χρήση του μέλους, χωρίς να επηρεάζονται άλλες δραστηριότητες, πχ η χρήση του χεριού κατά το φαγητό. Η μορφή αυτή της δυστονίας, θεωρείτο ψυχογενής για πολλά χρόνια, σήμερα, όμως, γνωρίζουμε ότι μηχανισμοί που σχετίζονται με την πλαστικότητα του εγκεφάλου σχετίζονται με την παθοφυσιολογία της κατάστασης αυτής.
Οι γενετικές (κληρονομικές) δυστονίες περιλαμβάνουν ένα μακρύ κατάλογο δυστονιών με διαφορετικά εμπλεκόμενα γονίδια και μπορεί να είναι αμιγείς δυστονίες ή συνοδευόμενες και από άλλα συμπτώματα και σημεία. Συνήθως εμφανίζονται σε νεαρές ηλικίες και η έναρξη είναι συνήθως από τα κάτω άκρα, με τάση για γενίκευση. Είναι πολύ σημαντικό να αντιμετωπίζονται από εξειδικευμένο νευρολόγο, μια και σε κάποιες από αυτές η έγκαιρη διάγνωση και η δέουσα αντιμετώπιση, είναι καθοριστικές για την πρόγνωση. Τέτοια είναι η περίπτωση της δυστονίας που απαντά στην ντόπα (Dopa Responsive Dystonia) και της νόσου του Wilson που μπορεί να αντιμετωπισθεί ικανοποιητικά αν διαγνωσθεί ή να οδηγήσει σε απειλητικές για τη ζωή καταστάσεις, αν μείνει χωρίς αντιμετώπιση.
Είναι χαρακτηριστικό το γεγονός ότι η δυστονία, λόγω της ιδιομορφίας της κλινικής της εικόνας, για δεκαετίες θεωρείτο ψυχογενής διαταραχή, με συνέπεια να έχει αντιμετώπιση από ψυχιάτρους. Σήμερα, γνωρίζουμε ότι (πέρα από ελάχιστες περιπτώσεις ψυχογενούς δυστονίας), η δυστονία είναι οργανική διαταραχή, συχνά με γονιδιακό υπόβαθρο και μπορεί να αντιμετωπιστεί από εξειδικευμένους στις διαταραχές κινητικότητας νευρολόγους.
Χαρακτηριστική είναι η διατήρηση συγκεκριμένου μοτίβου κινήσεων, ανεξάρτητα αν αυτές είναι αργές ή πιο γρήγορες.
Συχνά η δυστονία συνοδεύεται από τρόμο (τρέμουλο), που μπορεί να αφορά την περιοχή του σώματος που πάσχει ή άλλες περιοχές π.χ μπορεί να έχουμε τρόμο χειρών σε αυχενική δυστονία.
Υπάρχουν πολλά είδη δυστονίας: μπορεί να είναι συνεχής ή με διακυμάνσεις, πρωτοπαθής ή δευτεροπαθής, κληρονομική ή σποραδική, να εμφανίζεται σε παιδική ηλικία ή μετά την ενηλικίωση, να εμφανίζεται σε κίνηση ή σε ηρεμία, να είναι περιορισμένη σε ένα μέρος του σώματος ή να είναι γενικευμένη.
Ίσως οι συχνότερες μορφές δυστονίας είναι οι σποραδικές, εστιακές δυστονίες. Η αυχενική δυστονία ή σπασμωδικό ραιβόκρανο (εικ 1) εμφανίζεται κατά τι συχνότερα σε γυναίκες, μέσης ηλικίας. Συνήθως, εμφανίζεται με κάμψη και στροφή της κεφαλής προς μία πλευρά, ενίοτε με ανύψωση του σύστοιχου ώμου και στροφή του πηγουνιού προς αυτόν. Μπορεί να συνοδεύεται από κάμψη της κεφαλής προς τα πίσω ή προς τα εμπρός. Σπάνια η κεφαλή μπορεί να πάρει μια σταθερή θέση, συνήθως οι συσπάσεις των μυών του αυχένα προκαλούν τρομώδη κίνηση της κεφαλής. Σε λιγότερο από 10% των ασθενών μπορεί να υπάρξει αυτόματη ύφεση των συμπτωμάτων μέσα στα πρώτα τρία χρόνια, στους περισσότερους, όμως, ασθενείς μπορεί να διαρκέσει εφ’ όρου ζωής. Η αιτιολογία δεν είναι γνωστή, αν και υπάρχουν πολλές θεωρίες που εμπλέκουν διαταραχές στην προσαγωγή αιθουσαίων ερεθισμάτων, γενετικούς παράγοντες, περιφερικό τραύμα κτλ. Μέχρι σήμερα, η καλύτερη αντιμετώπιση της κατάστασης είναι με ενέσεις αλλαντικής τοξίνης (Bot. Tox), από εξειδικευμένο στις διαταραχές κινητικότητας νευρολόγο.
Ο βλεφαρόσπασμος, μια άλλη μορφή εστιακής δυστονίας, χαρακτηρίζεται από σπασμωδικές συσπάσεις του σφικτήρα των βλεφάρων, που μπορεί να συνοδεύεται από συσπάσεις και άλλων μυών του προσώπου ή του στόματος.
Συνήθως, επιδεινώνεται με το δυνατό φως, τον αέρα, τις κινήσεις και το στρες. Μπορεί να οδηγήσει σε προβλήματα στην καθημερινή ζωή, αφού μπορεί να οδηγήσει, ακόμα και σε δυσκολία του ασθενή να διασχίσει το δρόμο. Ο πρωτοεμφανιζόμενος βλεφαρόσπασμος, πρέπει να διαφοροδιαγνωσθεί από άλλες καταστάσεις, που μπορεί να προκαλούν πτώση βλεφάρου, καθώς και από δευτεροπαθή βλεφαρόσπασμο, που μπορεί να οφείλεται σε δομικές βλάβες. Ο θεράπων νευρολόγος, κρίνει και αποφασίζει την διενέργεια μαγνητικής τομογραφίας εγκεφάλου για αποκλεισμό τέτοιων βλαβών. Η αντιμετώπιση είναι και σε αυτήν την εστιακή δυστονία με ενέσεις αλλαντικής τοξίνης (Bot. Tox), από εξειδικευμένο στις διαταραχές κινητικότητας νευρολόγο.
Ιδιαίτερη κατηγορία εστιακής δυστονίας είναι η σχετιζόμενη με την πράξη, όπως η δυστονία γραφέως και άλλες επαγγελματικές δυστονίες, όπως η δυστονία των μουσικών. Αυτές εμφανίζονται σε ασθενείς, που χρησιμοποιούν υπερεντατικά το προσβεβλημένο μέλος, για συγκεκριμένη δραστηριότητα, όπως γραφή ή τη χρήση μουσικών οργάνων.
Η δυστονία αφορά μόνο στη συγκεκριμένη χρήση του μέλους, χωρίς να επηρεάζονται άλλες δραστηριότητες, πχ η χρήση του χεριού κατά το φαγητό. Η μορφή αυτή της δυστονίας, θεωρείτο ψυχογενής για πολλά χρόνια, σήμερα, όμως, γνωρίζουμε ότι μηχανισμοί που σχετίζονται με την πλαστικότητα του εγκεφάλου σχετίζονται με την παθοφυσιολογία της κατάστασης αυτής.
Οι γενετικές (κληρονομικές) δυστονίες περιλαμβάνουν ένα μακρύ κατάλογο δυστονιών με διαφορετικά εμπλεκόμενα γονίδια και μπορεί να είναι αμιγείς δυστονίες ή συνοδευόμενες και από άλλα συμπτώματα και σημεία. Συνήθως εμφανίζονται σε νεαρές ηλικίες και η έναρξη είναι συνήθως από τα κάτω άκρα, με τάση για γενίκευση. Είναι πολύ σημαντικό να αντιμετωπίζονται από εξειδικευμένο νευρολόγο, μια και σε κάποιες από αυτές η έγκαιρη διάγνωση και η δέουσα αντιμετώπιση, είναι καθοριστικές για την πρόγνωση. Τέτοια είναι η περίπτωση της δυστονίας που απαντά στην ντόπα (Dopa Responsive Dystonia) και της νόσου του Wilson που μπορεί να αντιμετωπισθεί ικανοποιητικά αν διαγνωσθεί ή να οδηγήσει σε απειλητικές για τη ζωή καταστάσεις, αν μείνει χωρίς αντιμετώπιση.
Είναι χαρακτηριστικό το γεγονός ότι η δυστονία, λόγω της ιδιομορφίας της κλινικής της εικόνας, για δεκαετίες θεωρείτο ψυχογενής διαταραχή, με συνέπεια να έχει αντιμετώπιση από ψυχιάτρους. Σήμερα, γνωρίζουμε ότι (πέρα από ελάχιστες περιπτώσεις ψυχογενούς δυστονίας), η δυστονία είναι οργανική διαταραχή, συχνά με γονιδιακό υπόβαθρο και μπορεί να αντιμετωπιστεί από εξειδικευμένους στις διαταραχές κινητικότητας νευρολόγους.
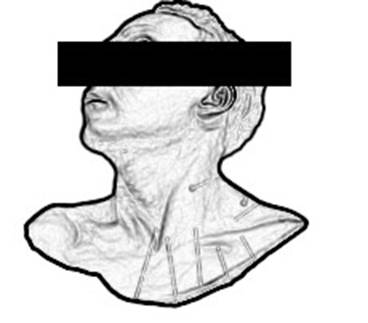
εικ. 1 αυχενική δυστονία ή σπασμωδικό ραιβόκρανο

εικ. 2 δυστονία κάτω άκρου στα πλαίσια γενετικής δυστονίας
►
▼
Η Χορεία
Η χορεία χαρακτηρίζεται από άρρυθμες, απρόβλεπτες, σύντομες, απότομες κινήσεις, που μετακινούνται διαρκώς από ένα σε άλλο μέρος του σώματος. Συχνά ο ασθενής δεν καταλαβαίνει τις κινήσεις αυτές και μας τις περιγράφει ή μας φέρνει τον ασθενή ο συνοδός.
Πολύ σημαντικό στην εξέταση ασθενούς με χορεία είναι το ιστορικό, αφού πχ ιστορικό στρεπτοκοκκικής λοίμωξης μπορεί να δηλώνει χορεία Sydenham, χορεία στη διάρκεια της εγκυμοσύνης μπορεί να δηλώνει Συστηματικό Ερυθηματώδη Λύκο ή αντιφωσολιπιδικό σύνδρομο, ενώ το κληρονομικό ιστορικό μπορεί να δηλώνει νόσο Huntington ή συναφή νοσήματα. Φάρμακα όπως τα νευροληπτικά και τα αντισυλληπτικά μπορεί, επίσης να αποτελούν αίτια.
Βαρύτερος από τη χορεία, αλλά μέσα στο φάσμα της είναι ο βαλλισμός, που χαρακτηρίζεται από μεγάλου εύρους, βίαιες, απότομες κινήσεις και εμφανίζεται συνήθως σε αγγειακά στον υποθαλάμιο πυρήνα, με την μορφή του ημιβαλλισμού. Οι αθετωσικές κινήσεις είναι βραδείες, άρρυθμες ερπυστικές κινήσεις – μεταξύ χορείας και δυστονίας.
Πολύ σημαντικό στην εξέταση ασθενούς με χορεία είναι το ιστορικό, αφού πχ ιστορικό στρεπτοκοκκικής λοίμωξης μπορεί να δηλώνει χορεία Sydenham, χορεία στη διάρκεια της εγκυμοσύνης μπορεί να δηλώνει Συστηματικό Ερυθηματώδη Λύκο ή αντιφωσολιπιδικό σύνδρομο, ενώ το κληρονομικό ιστορικό μπορεί να δηλώνει νόσο Huntington ή συναφή νοσήματα. Φάρμακα όπως τα νευροληπτικά και τα αντισυλληπτικά μπορεί, επίσης να αποτελούν αίτια.
Βαρύτερος από τη χορεία, αλλά μέσα στο φάσμα της είναι ο βαλλισμός, που χαρακτηρίζεται από μεγάλου εύρους, βίαιες, απότομες κινήσεις και εμφανίζεται συνήθως σε αγγειακά στον υποθαλάμιο πυρήνα, με την μορφή του ημιβαλλισμού. Οι αθετωσικές κινήσεις είναι βραδείες, άρρυθμες ερπυστικές κινήσεις – μεταξύ χορείας και δυστονίας.
►
▼
Ο Μυόκλονος
Ο μυόκλονος χαρακτηρίζεται από απότομες, αστραπιαίες, σύντομες ακούσιες κινήσεις. Μπορεί να είναι φυσιολογικός (νυχτερινός, λόξυγγας), ιδιοπαθής (μυοκλονική δυστονία), επιληπτικός, συμπτωματικός (όπως σε προϊούσες εγκεφαλοπάθειες ή σε άνοιες) ή μεταβολικός (νεφρική ή ηπατική ανεπάρκεια, υποξία κτλ). Από πλευράς φαινομενολογίας διακρίνεται ανάλογα με το εύρος του, την κατανομή του (εστιακός, τμηματικός …), τη συμμετρία του (συμμετρικός ή ασύμμετρος) και τις συνθήκες εμφάνισής του (αυτόματος ή προκλητός από ερεθίσματα πχ κίνηση, θόρυβο, φως).
►
▼
Τα Τικς
Τα τικς είναι σύντομες και διακοπτόμενες κινήσεις (κινητικά τικς) ή ήχοι (φωνητικά τικς). Τα κινητικά τικς είναι απότομες, σύντομες, παροδικές και συχνά επαναλαμβανόμενες κινήσεις, που μπορεί να μιμούνται χειρονομίες ή φυσιολογικές συμπεριφορές και επαναλαμβάνονται με ακανόνιστο τρόπο. Οι ασθενείς αισθάνονται μια ακατανίκητη ανάγκη να κάνουν τις κινήσεις, ή ένα περίεργο τοπικό αίσθημα, που υποχωρεί μερικώς μετά την κίνηση. Μπορούν να καταπιεστούν, αλλά δύσκολα λόγω αυτής της ανάγκης και αυξάνουν με το στρες. Τα τικς μπορεί να είναι απλά ή σύνθετα και μπορεί να συνοδεύονται από καταναγκασμούς, κοπροπραξία, ηχοπραξία, σύνδρομο διάσπασης προσοχής και αυτοκαταστροφική συμπεριφορά.
►
▼
Ο τρόμος
Ο τρόμος είναι η ρυθμική κίνηση ενός μέλους του σώματος, που προκαλείται από σύγχρονες ή εναλλασσόμενες συσπάσεις αγωνιστών – ανταγωνιστών μυών. Συνήθως έχει σταθερή συχνότητα αν και το εύρος του μπορεί να μεταβάλλεται ανάλογα με την ψυχική κατάσταση του ασθενούς ή άλλους παράγοντες. Παρότι ο τρόμος της νόσου του πάρκινσον είναι ο γνωστότερος, ο ιδιοπαθής τρόμος, που είναι καλοήθης κατάσταση είναι πολύ συχνότερος. Είναι κληρονομικός και βελτιώνεται πολύ με το αλκοόλ. Υπάρχουν πολλά ακόμη είδη τρόμου, με διαφορετικά αίτια. Απαραίτητη είναι η εκτίμηση του νευρολόγου, όταν αυτά εμφανίζονται, ώστε να γίνει η εκτίμηση και αν χρειάζεται η αντιμετώπισή τους.

